-
 Hola, estoy estudiando quimica organica y no sé qué signifacan algunas letras que se ponen delante del nombre del compuesto.
Hola, estoy estudiando quimica organica y no sé qué signifacan algunas letras que se ponen delante del nombre del compuesto.Gracias.


José Miguel
el 5/2/17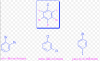 Hola Sofía, las letras que indicas son: o- que proviene de orto, y p- que proviene de para. Son unos prefijos usados de manera común en compuestos cíclicos en química orgánica (existe otro que también encontrarás: m- que proviene de meta). Indican las posiciones de dos de los sustituyentes en un ciclo: orto indica posiciones 1,2; meta se refiere a posiciones 1,3; y para hace referencia a sustituyentes en posiciones 1,4.
Hola Sofía, las letras que indicas son: o- que proviene de orto, y p- que proviene de para. Son unos prefijos usados de manera común en compuestos cíclicos en química orgánica (existe otro que también encontrarás: m- que proviene de meta). Indican las posiciones de dos de los sustituyentes en un ciclo: orto indica posiciones 1,2; meta se refiere a posiciones 1,3; y para hace referencia a sustituyentes en posiciones 1,4.Saludos.
-
¿Alguien me puede echar una mano con un ejercicio de química de estequiometria?
El enunciado es el siguiente:
Habitualmente el carbono reacciona con el oxígeno para dar dióxido de carbono. Pero cuando no hay carbono suficiente, la reacción produce monóxido de carbono.
Me piden las moléculas de oxígeno que deben reaccionar para que 1kg de carbono se transforme íntegramente en cada una de esas sustancias.
Y después la presión que ejercería el monóxido o dióxido de carbono que se supone que he calculado si la combustión se produce en una habitación de 3m x 4m x 2.5m que se encuentra a 25ºC
Tengo este problema porque vine de estudiar en el extranjero y esto no lo di, y mi profesora se niega a explicármelo, no os pido que me resolvais el ejercicio entero, simplemente quiero saber como hacerlo, o entenderlo, gracias de antemano.


David
el 5/2/17C(s) + O2(g) = CO2(g) Y a partir de ahí, estequiometria... Estequiometria 01 Pasa los 1000 gramos de C a moles, y con ellos los moles de O2 y de CO2...
Recuerda además que P.V=n.R.T... el volumen de la habitacion es 3.4.2,5=30 m³= 30000 dm³= 30000 litros. Gases ideales PV=nRT
A partir de ahí, se trata de que DESPUES DE IR A CLASE (ver los vídeos relacionados con vuestras dudas) enviéis dudas concretas, muy concretas. Y que nos enviéis también todo aquello que hayais conseguido hacer por vosotros mismos. Paso a paso, esté bien o mal. No solo el enunciado. De esa manera podremos saber vuestro nivel, en que podemos ayudaros, cuales son vuestros fallos.... Y el trabajo duro será el vuestro. Nos cuentas ¿ok? #nosvemosenclase ;-) -
Hola un saludo a todos, ¿alguien podria decirme como se hace este ejercicio? """ El peróxido de bario (BaO2) se descompone dando el óxido normal (BaO) y desprendiendo oxígeno. ¿Qué cantidad en tanto por ciento supone esta descomposición? """"" Me trae de cabeza. Gracias.
-
hola soy nueva me quiero presentar a selectividad por quimica y me gustaria saber por donde empezar a prepararme. un saludo gracias


José Miguel
el 4/2/17Hola Nuria, si necesitas una buena base te recomiendo que en la sección de química empieces por el principio, desde nivel ESO hasta 2º de bachiller. Si ves que hay cosas muy básicas porque ya tienes cierto nivel te las puedes saltar.
El enlace está en la parte superior de la página: "vídeos", por asignaturas, "química" y manos a la obra, cualquier duda por aquí estamos.
Saludos.
-
Buenas tardes, quería preguntaros sí tenéis algún video de cómo calcular cúando un ácido es fuerte o débil al igual que una base. Sería a nivel de 4º de la ESO.
Gracias
Rocío

Gabriel
el 4/2/17Hola Rocio. En este caso es según los datos que se den o en caso calcular la constante de acidez o basicidad. Si tenemos una constante Ka o Kb alta, entre 10-3 y 1, es una base o ácido fuerte. Otra forma más sencilla es viendo su ph. Si tenemos un ácido con un ph entre 0 y 3 es fuerte y una base con un ph entre 10 y 14 es fuerte, puesto que ph=7 es neutro.
Espero haber sabido expresarme con claridad
-
Buenas tardes, ¿me podrían explicar cómo hacer este ejercicio de disoluciones?:
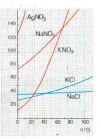
a) Calcular cuantos gramos de cloruro de potassio, KCl, se pueden disolver como máximo en 500 g de agua a 50ºC.
b) Si la disolución anterior se enfría a 20ºC, ¿cuantos gramos de KCl se depositarán en el fondo?
Soluciones: a) 205 g de KCl
b) 45 g de KCl
Usuario eliminado
el 3/2/17Hola buenas tardes,
para realizar este ejercicio debes buscar un diagrama de solubilidades en el que aparezca el KCl. En éste, debes ver la solubilidad de la substancia a diferentes temperaturas. A partir de aquí, mediante un factor de conversión puedes saber la masa de KCl que se puede disolver en 500g de agua a 50ºC. Para el apartado b) debes calcular la masa que se puede disolver a 20ºC y la diferencia de masa respeto a la situación anterior será la masa de KCl que se depositará en el fondo.
Saludos,
Roger Monreal
-
Buenas tardes,
Estaba haciendo el ejercicio 8, de la hoja 127, y tengo una duda con la variación en el número de moles gaseosos.. a mí me sale -1 porque tenemos 4 del agua + 3 del dióxido de carbono menos 1 del propano y 5 del oxigeno. (3+4)-(1+5)=-1 en cambio en el ejercicio pone variacion -3... y no veo el porque... si me pudieseis ayudar.. muchas graciasss :)