-
 Hola ayuda con este ejercicio por favor, quería ver si esta bien lo planteado por mi por que la pauta me dice otra cosa, saludos
Hola ayuda con este ejercicio por favor, quería ver si esta bien lo planteado por mi por que la pauta me dice otra cosa, saludosÁngel
el 15/8/17Según Bohr, un átomo con:
1 nivel de energía hay un máximo de 2 electrones
2 niveles de energía hay un máximo de 8 electrones
3 niveles de energía hay un máximo de 18 electrones
4 niveles de energía hay un máximo de 32 electrones
.
.
x niveles de energía hay un máximo de 2x2 electrones
Lo tienes bien resuelto.
-
Hola
Sguramente no es el mejor sitio para esto, pero no he encontrado un e-mail o formulario de contacto
Quisiera informar al webmaster/s de que justo hoy se os caducado el certificado de la página web unicoos.com por lo que algunos navegadores ni si quiera dejan acceder y otros dan fallos de seguridad impidiendo el correcto seguimiento de las lecciones.
Espero que lo podáis solucionar pronto
Un saludo
-
Halla la variación de energía interna que sufre un mol de agua a 25ºC cuando se trasforma en vapor de agua a 125ºC, si la presión de 1 atm se mantiene constante.
Datos:
Ce : H2O (l): 4,18 J/gºC ; H2O (v): 1,92 J/gºC
L vaporización : 2,25.103 J/g
He realizado el ejercicio siguiendo los siguientes pasos, pero no me da la solución.
1º. He calculado cuantos g de agua hay en un mol, que son 18g.
2º. Al ser presión constante el W es igual a 0 (w = p • ΔV), por lo que ΔU = Q + W pasaría a ser ΔU = Q
3º. He hallado el calor que desprende en estado líquido (5643 J), gaseoso (864 J) y durante el cambio de estado (40500 J) con las siguientes fórmulas: Q = Ce • m • ΔT / Q = m • Lv
4º. He sumado todo el calor y lo he pasado a kJ, quedando una cifra de 47 kJ, que sería negativa dado que se desprende calor.
5º. Por lo que ΔU = - 47kJ.
La solución del libro es 43,7 kJ. ¿Dónde me he equivocado?
Muchas gracias.
Breaking Vlad
el 16/8/17Hola Esther,
En tu planteamiento veo dos fallos.
En primer lugar dices que es negativo dado que se desprende calor, lo cual es incorrecto, en todo ese procedimiento, lo que se está dando es absorción de calor, para evaporar el agua se ha de absorber calor, no desprenderlo.
En segundo lugar, al ser presión constante tienes:
W=P· ΔV, lo cual NO es igual a 0. el volumen varía, y la presión es distinta de 0, luego P · ΔV tendrá un valor determinado.
Este factor del trabajo puedes tenerlo solo en cuenta en el calentamiento en fase gas, ya que la expansión del agua líquida será prácticamente despreciable, así que para P·ΔV deberás tener en cuenta el volumen de gas a 125 y el volumen de gas a 100
Espero haberte ayudado un poquito,
un saludo,
Breaking Vlad
-
hola buenos días.
resulta que hay un ejercicio de un examen de 2º Eso de física y química que no entiendo.
el enunciado dice así:
*calcula las cantidades de cloro y sodio que hay que hacer reaccionar para obtener 500 gramos de sal (cloruro sódico).
Mat (CL) = 35, 5 uma ; Mat (Na)= 23 uma
y no me dice nada mas, ¿alguien me puede ayudar?
Breaking Vlad
el 15/8/17Hola Enrique,
En ese ejercicio se da por sentado que sabes cuál es la reacción de formación del NaCl (cloruro sódico) de modo, que imagino que os la habrán explicado en teoría.
La reacción sería esta:
2Na + Cl2 -> 2NaCl
Intenta resolver con estos datos el ejercicio, y cualquier duda que te surja, aquí estamos para ayudarte. (Eso sí, recuerda que no resolvemos vuestros ejercicios, sino que os ayudamos a resolverlos vosotros mismos)
Un saludo,
Breaking Vlad
-
Hola, yo diría que tal y como hice el ejercito esta bien pero siempre este esa duda 😌 serias tan amable de decirme si esta bien o mal?

Breaking Vlad
el 14/8/17Piotr
el 14/8/17 -
Hola Unicoos,
En los problemas de reactivo limitante, siempre hay que probar con las dos masas de los reactivos para ver qué valor es menor y hallar el reactivo como he hecho en este ejercicio? No hay otra forma de saber cuál es el reactivo?
Y por último, me podrían explicar lo de las cifras significativas, porque en estos tipos de problemas creo que hay que fijarse en las cifras decimales que te da el enunciado y después tú debes operar con determinadas cifras pero eso yo no lo comprendo .
MUCHAS GRACIAS
Breaking Vlad
el 14/8/17Hola Lbp,
Te comento, el reactivo limitante puede hallarse de varias maneras, una de ellas es la que tú has señalado.
Sin embargo, yo utilizo generalmente otra. En ese ejercicio por ejemplo, te dan masa de SiO2, y la masa de C.
Con eso calculas los moles de SiO2 y los moles de C. Sabiendo que el ratio es SiO2 : C es 1 : 3, puedes comparar.
Por ejemplo, imagínate que te diera 0,35mol de SiO2 y 1,5mol de C. En esta mezcla hay más C de la cuenta, con lo que el limitante es el SiO2.
En cuanto a tu duda de las cifras significativas te recomiendo que postees la pregunta en el foro de matemáticas que allí sabrán ayudarte mejor con este tema ;)
Espero haberte aclarado un poco la duda,
un saludo,
Breaking Vlad
-
buenas, agradeceria un monton que me ayudaseis con este problema porque no consigo resolverlo. Muchas gracias :))
Breaking Vlad
el 14/8/17Se trata de que DESPUES DE IR A CLASE (ver los vídeos relacionados con vuestras dudas) enviéis dudas concretas, muy concretas. Y que nos enviéis también todo aquello que hayais conseguido hacer por vosotros mismos. Paso a paso, esté bien o mal. No solo el enunciado. De esa manera podremos saber vuestro nivel, en que podemos ayudaros, cuales son vuestros fallos.... Y el trabajo duro será el vuestro. Nos cuentas ¿ok? #nosvemosenclase ;-)
-
Hola, buenas, tengo una duda
al hace configuración R y S el sustituyente de menor importancia pasa detrás, pero el resto qu hago con ellos? Gracias
Breaking Vlad
el 12/8/17Hola Alex,
Antes de nada, comentarte que en los foros de unicoos no respondemos preguntas universitarias, sin embargo, te comparto este vídeo mio en el que explico como hallar la configuración R o S en los compuestos quirales.
Un saludo,
Breaking Vlad
José Miguel
el 12/8/17Buenas tardes, permitidme intervenir diciendo que es de gran utilidad para los cursos en los que se trata la estereoisomería (normalmente en la universidad) hacerse con maquetas de modelos moleculares. Éstas están compuestas por barras y bolas de distintos colores que representan los distintos átomos. A mi me resultaron muy instructivas a pesar de no tener problemas de visión espacial, sobretodo a la hora de explicar este tema a los compañeros que más dificultades tenían.
Un saludo Álex, y otro para Breaking Vlad :)
Alex Domínguez
el 12/8/17José Miguel
el 12/8/17Hola Alex, a pesar de las limitaciones a las que nuestra sociedad nos someta, la imaginación es una buena compañera. Si dispones de palillos de madera, y plastilina o cualquier otro material moldeable para transformar en una bola, tú mismo puedes crear tus propios modelos :)
Un saludo.
Breaking Vlad
el 12/8/17Totalmente de acuerdo con José Miguel,
Los modelos moleculares son una herramienta crucial para quien no tiene vision espacial.
Sin embargo, también te voy a recomendar otra herramienta. Parece que PC sí que tienes (por participar en el foro). para PC tienes disponibles herramientas gratuitas como Jmol, o Avogadro, que son softwares en los que puedes construir moléculas tridimensionales y eso te puede ayudar a visualizar las moléculas sin necesidad de comprar nada.
Un saludo Álex y José Miguel,
Breaking Vlad
-
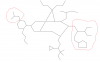
Hola, tengo duda en cómo se nombran estos dos sustituyentes marcados en rojo del Biciclo, ya que por un lado tengo un ciclohexil como sustituyente del biciclo, pero este ciclohexil posee sustituyentes, uno de ellos sería un 5-(2-metilpropil), entonces no se si se pueda nombrar así el sustituyente completo del carbono nro 8 del biciclo : 8-(2-butil-5-(2-metilpropil)ciclohexil) con dos paréntesis dentro del nombre. y el caso del otro sustituyente en rojo la misma historia. Si no es así, me pueden decir cómo sería correctamente la nomenclatura de éstos porfavor.
José Miguel
el 12/8/17Hola Jorge, en cuanto al que tienes rodeado en la parte izquierda, sería un isobutil- , y también aceptado, aunque más largo: (2-metil)propil-. El sustituyente completo sería: 2-butil-5-isobutilciclohexil-
En cuanto al marcado a la derecha, me arriesgaría a nombrarlo, con cierta seguridad, de la siguiente manera:
(2-ciclopentil etil)-3-etilpentil-
Espero haberte ayudado.
Saludos.