-
Según lo que he visto en videos explicativos sobre el cáculo de la fuerza electromotriz en una pila Daniel, en el ánodo hay que colocar el elemento con mayor fuerza electromotriz y en el cátodo el de menor. Pues no entiendo por qué con estos datos,
Datos: Eº(Cu2+/Cu)= +0,34 V y Eº(Zn2+/Zn)= -0,76 V. Me pusieron en un examen que la respuesta correcta es: Las reacciones que tienen lugar son:
Cu2+ (ac) + 2e- → Cu(s) Eº=0,34V. Redución: cátodo
Zn(s) → Zn2+ (ac)+ 2e– Eº=0,76VOxidación: ánodo
Zn + Cu2+→ Zn2+ + Cu Eº=1,10V
-
Buen día, me explicarían este problema? Por favor. Una muestra que contiene NaCl, NaBr, NaI y materia inerte que pesa 1,500 g se disuelve en agua y se lleva a un volumen de 100 mL en un matraz aforado. Una porción alícuota de 50,0 mL dió un precipitado de yoduro de paladio (II), PdI2, que pesó 0,1103 g. Una segunda alícuota de 50,0 mL tratada con una solución de nitrato de plata, arrojó un precipitado de los haluros de plata de 1,2312 g. El segundo precipitado se calentó en una corriente de cloro, con lo que el bromuro y el yoduro de plata se convirtieron en cloruro de plata que pesó 1,0500 g. Calcule el porcentaje de cada componente en la muestra. (12,21 % NaI, 38,62 % NaBr, 30,37% NaCl)
-
Hola, ¿me podrían ayudar con un ejercicio que dice así?:
¿Qué volumen de agua habrá que añadir a 50 mL de disolución de ácido clorhídrico, HCL, del 37,2% de riqueza y 1,19 g/mL de densidad para obtener una disolución 1,5M?
Datos: Masas molares: H = 1g/mol;Cl=35,5g/mol.
Por favor no quiero que me lo resuelvan sino que me lo expliquen. Gracias de antemano y un saludo!
-
-
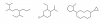
Buenas, ¿me podéis decir si he nombrado correctamente los compuestos que adjunto (están en orden)?
a) 6-(1-metilpropil)-2,3-dimetilnonano
b) 1-cloro-3-etil-4-isopropilciclohexano
c) 1-(2-metilciclopentil)-5-ciclopropilciclodecano
-
Alguien sabe si para nombrar REACCIONES QUÍMICAS debo utilizar la nomenclatura sistemática/de combinación, o debo usar otra?
URGENTEEE por favor
-

Diego Cdb
el 15/3/17A ver, te lo intento explicar. Deberías saber que en una reacción irreversible como la que tú planteas, la velocidad de reacción es igual a la constante de reacción k por las concentraciones de reactivos elevadas a sus órdenes de reacción (v=k[A]^a*[B]^b)
En tu caso, por tanto, el apartado a) se resolvería así: v=k[A][B]^2
El orden total de reacción es la suma de los órdenes parciales de los reactivos. En tu caso, a+b=3
Espero haberte sido de ayuda
-
¿Alguien sabría resolver el siguiente problema de 2º de bachillerato?: El hidróxido de cadmio (II) es una sustancia cuyo producto de solubilidad es 7,2x10^-15 a 25ºC, y aumenta con la temperatura. Justifica si son verdaderas o falsas las siguientes afirmaciones: a) El proceso de solubilización de esta sustancia es exotérmico. b) La solubilidad a 26ºC tiene un valor de 1,24x10^-5 g/L. c) Esta sustancia se disuelve más fácilmente si se reduce el pH del medio.
-
Hola, podría explicarme cómo se resuelve este ejercicio: “ Al analizar dos óxidos de cromo se comprueba que en 5 g del primer óxido hay 3,82 g de cromo y que en 5 g del segundo óxido, hay 2,60 g de cromo. Comprueba que se cumple la ley de las proporciones múltiples”
Gracias
-