-
Buenas, alguien me podría explicar que es la solubilidad y un ejemplo me serviría de mucha ayuda. Gracias.
Guillem De La Calle Vicente
el 1/1/17La solubilidad de un soluto en un disolvente se define como la concentración que tiene el soluto dentro del disolvente cuando la disolución está saturada, mesurada a una temperatura determinada.
Si analizamos el proceso de disolución de un sólido iónico, podemos comprobar que, porque una sal se disuelva, se han de vencer las atracciones entre los diferentes iones que forman el sólido; por lo tanto, se tiene que romper la red cristalina.
Este proceso requiere una aportación energética equivalente a la energía reticular del sólido iónico, aportación que se ve compensado por la energía de atracción entre los iones y las moléculas polares del disolvente. Generalmente, el disolvente es el agua, y en este caso el proceso se conoce con el nombre de hidratación.
Teniendo en cuenta este concepto:
- Una sustancia soluble es la que tiene una energía reticular que puede ser compensada con una energía de hidratación relativamente grande.
- Una sustancia insoluble es la que tiene una energía reticular muy grande que no se compensa con la energía de hidratación.
La mayoría de las disoluciones de sustancias sólidas son procesos endotérmicos y de aumento de entropía. Por cada temperatura se estable un equilibrio de solubilidad.
Experimentalmente, se puede comprobar, que, para la mayoría de las sustancias sólidas, a más temperatura, más solubilidad, i la disolución también tiene lugar más rápidamente. Por ejemplo, el azúcar es fácilmente soluble en leche calienta, mientras que la leche fría dificulta la disolución. Por tanto, las temperaturas altas favorecen el proceso de disolución.
-
¿Podría alguien echarme una mano con este problema? Muchas gracias.
Dice así (Equilibrio químico, Química 2ºBachillerato): Se introducen 0,25 moles de dióxido de carbono en un recipiente de dos litros a una temperatura de 1023 K. A esta temperatura el compuesto se descompone parcialmente según la reacción: 2CO2 ---> <---- (doble sentido) 2CO (g) + O2 (g)
La concentración de monóxido de carbono en el equilibrio es 0,40 mol/L. Calcula las concentraciones de los compuestos en el equilibrio, Kp y Kc.
Dato: R = 0,82 atm L /mol K
En primer lugar, como es una reacción de equilibrio, definimos los estados iniciales y de equilibrio con sus respectivas incógnitas:
2CO2 ----> <---- (doble sentido) 2CO2 + O2
i) 0,25 mol _ _
eq) 0,25 - 2x 2x x
(Pongo moles, no concentraciones).
Dado que hay 0,40 moles de CO2 en el equlibrio, y concentración = nº moles / volumen ---> 0,40 = nºmoles / 2 ---> moles = 0,80 moles de CO2 en el equilibrio.
Ahora me quedo atascada pues no me cuadra que de 0,25 moles que hay al inicio en los reactivos, de repente haya 0,80 moles en uno de los productos. Como los moles no pueden formarse "mágicamente", lo único que se me ocurre es que haya una cantidad "z" de moles en los productos al inicio. ¿Es eso posible? Además traté de resolver así el problema y z me daba igual a x (daba 0,40, pero de nuevo no cuadra, pues al restarle a 0,25 moles, 0,40 moles, da -0,15 moles..).
¿Me podéis echar una mano?
Muchas gracias y Feliz Año! :)
-
David
el 2/1/17Te sugiero este video... Ajustar una reacción en medio acido - Ion-electron
A partir de ahí, se trata de que DESPUES DE IR A CLASE (ver los vídeos relacionados con vuestras dudas) enviéis dudas concretas, muy concretas. Y que nos enviéis también todo aquello que hayais conseguido hacer por vosotros mismos. Paso a paso, esté bien o mal. No solo el enunciado. De esa manera podremos saber vuestro nivel, en que podemos ayudaros, cuales son vuestros fallos.... Y el trabajo duro será el vuestro. Nos cuentas ¿ok? #nosvemosenclase ;-) -
Hola, me gustaría saber si hay vídeos sobre sales binarias y sales dobles.
Muchas gracias por todos tus vídeos, gracias a ellos me entero mejor y obtengo mejores calificaciones ya que me son de gran utilidad. Enhorabuena por la nominación a los TeacherPrize!
Ángel
el 31/12/16
-
Guillem De La Calle Vicente
el 29/12/16 -
Alguien me puede ayudar?
2) Isomería:
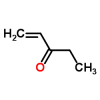
a) (0,5 puntos) Formula el compuesto etenilmetil éter (o etenoximetano) y formula y nombra un isómero de él que sea una cetona.
b) (0,5 puntos) ¿Por qué tiene isomería cis-trans el compuesto 1,2-dicloroeteno?
David
el 2/1/17¿Y cual es tu duda? Revisa este video... QUIMICA organica ETERES Y tambien estos Isomería
¿nos cuentas depsues? Se trata de que seáis vosotros quienes hagáis el trabajo duro y hagáis preguntas concretas
Besos! -
Gases-Leyes Ponderales y volumétricas. "Si se combinan 2L de N2 (gas) con 1L de O2 (gas), estando los dos en las mismas condiciones de presión y temperatura, se forman 2L de un gas, compuesto por ambos elementos, que se utiliza como anestésico. ¿Cuál es la fórmula de ese nuevo gas? Explica tu respuesta."
Solo sé que se cumple la Ley de los volúmenes de combinación, pero el resto ya no sé.
David
el 2/1/172N2 + O2 = 2 NxOy.... Por tanto... x=2, y=1... Te quedará... 2N2 + O2 = 2 N2O... de esa manera la reaccion queda ajustada y se cumple
Ley de GAY-LUSSAC o de los volúmenes de combinación -
Hola buenas, Unicoos
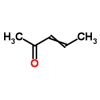
¿La pent-3-en-2-ona también puede ser llamada pent-3-enona?
Gracias
Guillem De La Calle Vicente
el 29/12/16Jesus Diaz Castro
el 29/12/16Guillem De La Calle Vicente
el 29/12/16 -
Hola queria preguntar si alguien me podria ayudar a este problema, lo he hecho pero en el corrector me dice que esta ajustada pero que no he tenido en cuenta que elemento tiene mayor tendencia a oxidarse.
El apartado b lo he calculado pero no me da, el resultado deberia ser 1,048 Voltios.
Gracias!
Una pila de botón está formada por dos electrodos uno de Pb/PbO y otro de Sn/SnO2 y un gel alcalino que actúa como electrolito. Se pide: a) Ajustar la reacción por el método del ión-electrón teniendo en cuenta que el Sn tiene una mayor tendencia a oxidarse. b) Calcular el potencial teórico de la pila.
DATOS: ∆GºPbO = -142,7 kJ/mol; ∆GºSnO2 = -689,7 kJ/mol; F = 96485 culombios
David
el 2/1/17Si nos envias al menos una foto con todo lo que conseguiste, el trabajo duro será el tuyo y podremos ayudarte mejor. Y saber donde fallas, que necesitas...
Fuerza electromotriz de una pila
Un abrazo!
Te sugiero además...Alexandru Simion
el 5/1/17http://i65.tinypic.com/14dimuf.jpg
Te adjunto el link de la imagen, ya que aqui quedaba muy grande, ese es el proceso que he utilizado, la he ajustado con metodo basico ya que es un gel alcalino, no se que puedo estar haciendo mal.
Un saludo.
Alexandru Simion
el 5/1/17Creo que ya he encontrado mi fallo, el enunciado dice que el Sn tiene mas tendencia a oxidarse, esto significa que la reaccion deberia ser: SnO2 > Sn así pues, el Sn estara dando electrones.
Mediante esta deducción he conseguido tener bien el ejercicio, si puedes afirmarmelo seria de agradecer. Un saludo!!